پردیس فناوری کیشطرح مشاوره متخصصین صنعت و مدیریتگروه مهندسی شیمی
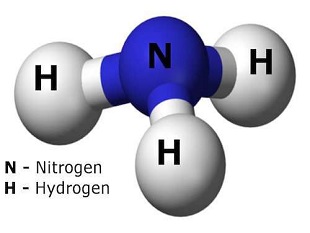
آمونیاک با فرمول شیمیایی NH۳، در هوای شهرها و مجاورت توالتها وجود دارد. در طبیعت از تجزیهٔ مواد آلی ازت دار همچون اوره ادرار بهدست میآید. رومیهای باستان آمونیوم کلرید را به عنوان پول و سپرده استفاده میکردند. آنها سنگ آمونیوم را از مکانی به نام پرستشگاه ژوپیتر یا همان لیبی جدید جمعآوری میکردند.
فرمول: NH3
فرمول مولکولی: NH3
شکل مولکولی: Trigonal pyramid
گشتاور دوقطبی: 1.42 D
دمای جوش: −33.34 °C, 240 K, -28 °F
مرتبط با nitrogen hydrides: هیدرازین; هیدرازوئیک اسید
دیگران این رومیهای باستان آمونیوم کلرید را به عنوان پول و سپرده استفاده میکردند. آنها سنگ آمونیوم را از مکانی به نام پرستشگاه ژوپیتر یا همان لیبی جدید جمعآوری میکردند. اما آمونیاک به شکل نمک آمونیاک نخستین بار توسط جابر ابن حیان در قرن ۸ شناخته شد.
تولیدگاز آمونیاک
روشهای صنعتی
مهمترین روش صنعتی تولید آمونیاک، فرایند هابر نام دارد که شامل تهیة آمونیاک از عناصر سازنده آن میباشد. در این روش، گازهای نیتروژن و هیدروژن در دمای بالا و در فشار زیاد با هم واکنش میدهند و آمونیاک را تولید میکنند. کاتالیزگرهای مختلف هم به سهولت این واکنش کمک مینمایندکاربرد
از موارد استفادهٔ آمونیاک میتوان به استفاده در تهیهٔ کودهای شیمیایی، یخ سازی، اسید نیتریک، سایر ترکیبات نیتروژنه، مواد منفجره و نگهداری از مواد غذایی اشاره کرد.
یکی دیگر از کاربردهای آمونیاک میتوان به استفاده در رشته ورزشی وزنهبرداری و پاورلیفتینگ اشاره نمود. بوییدن این محلول باعث بازکردن عروق میشود و ورزش کار را تا حدودی عصبی میکند و در مهار کردن وزنه در مسابقات کمک میکند.
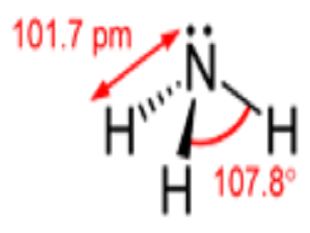
ساختار مولکولی
مولکول آمونیاک از یک اتم نیتروژن و سه اتم هیدروژن متصل به آن تشکیل شدهاست. با توجه به وجود یک جفت الکترون ناپیوندی بر روی نیتروژن، این مولکول ساختار هرم مثلثی دارد و زوایای پیوند کمتر از ۱۰۹ درجه هستند.[۷] مولکول آمونیاک یک مولکول قطبی است که میتواند با خودش و بسیاری مولکولهای دیگر، پیوند هیدروژنی برقرار نماید.
خصلت بازی
آمونیاک طبق نظریههای اسید و باز برونستد-لوری و لوویس، یک ترکیب بازی محسوب میشود. pH محلول آبی آن هم بیشتر از ۷ است که این واقعیت را آشکار میسازد. واکنش زیر، خصلت بازی مولکول آمونیاک را توضیح میدهد
واکنش تفکیک بازی آمونیاک:
(NH3(aq) + H2O(l) → NH4+(aq) + OH-(aq
